学部課程の熱力学や物理化学では、内部エネルギーを学習した後にエンタルピー(enthalpy)と呼ばれる示量性状態量を学習します。これは、相転移や化学反応などで物質の状態が変化する際に、化学ポテンシャルや内部エネルギーに体積の変化を加味した物理量です。これは、内部エネルギー(U)、圧力(p)、体積(V)の関係式で表わされます。この物理量の定義とは、H=U+pVとなります。Hの大きさや符号によって、化学反応や相転移などの“起こりやすさ”が決まります。
相転移や化学反応の際に体積の変化が起こらなければ、エンタルピーの変化は内部エネルギーの変化量と等しくなります。ただし体積や圧力も同時に変化するような場合は、化学ポテンシャル以外に体積と圧力(=仕事)を加えたトータルのエネルギーの出入りが発生します。
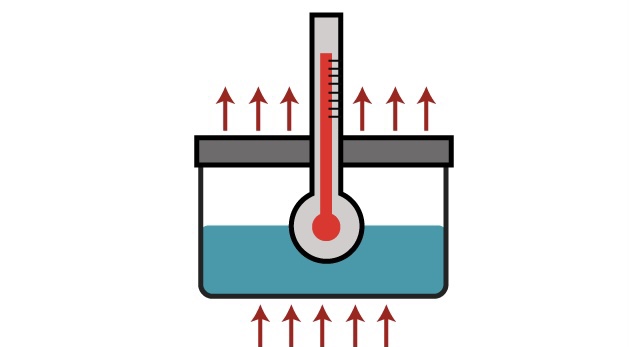
エンタルピーとは、物質が化学反応や相転移を起こして安定した状態に変化する際に、反応によって発生するトータルのエネルギーを表わすのに用いられます。反応により体積が増加する場合には、化学ポテンシャルによるエネルギー変化から、体積変化により外部に行う仕事に相当するエネルギーを差し引いた分が熱として外部に放出されることになります。
ここで分かりやすい例を考えてみると、紙や木材など(固体)や灯油(液体)などの有機物が空気中の酸素と結合した二酸化炭素と水蒸気(気体)になって膨張するようなケースを考えてみます。燃焼前の炭素や水素が酸素と結合して二酸化炭素や水に変化することで化学的に安定な状態になるので、酸化反応にともなってエネルギーが発生します。ただし、生成物(二酸化炭素と水蒸気)は気体として放出されるので、固体から気体になる際に非常に大きな体積の変化が生じます。大気中で気体を膨張させるためにはエネルギーを消費して外部に仕事をする必要がありますが、これには酸化反応によって発生するエネルギーの一部が使われます。そのため、燃焼により外部に放出される熱量は反応前後における化学物質の持つ内部エネルギー(化学ポテンシャル)の変化とは一致しません。
一般的に物質が化学反応や相転移などを起こす際は、外部に対する仕事(膨張または収縮)が起こるケースがほとんどです。反応の起こりやすさや発生する熱量は反応の前後の体積変化を考慮しなければならず、エンタルピーを用いる必要があります。ちなみにエンジン(内燃機関)では仕事を取り出す必要がありますが、このような場合にもエンタルピーが重要になります。
